垂盆草から得られる脂肪代謝改善剤、該脂肪代謝改善剤を含有する医薬又は食品、並びに垂盆草から得られる新規メガスチグマン及びフラボノイド化合物
【課題】ベンケイソウ科植物である垂盆草より得られる脂肪代謝改善剤、脂肪代謝改善効果を有するヒト又は動物用医薬もしくは食品、さらに、垂盆草の抽出成分を分離、精製することにより得ることができる新規メガスチグマン及びフラボノイド化合物を提供する。
【解決手段】垂盆草の全草、水もしくは低級脂肪族アルコールの含水物等により垂盆草を抽出して得られる抽出液、又は前記抽出液を濃縮して得られる抽出エキス、 又は該抽出液等を分離、精製して得られるメガスチグマン及びフラボノイド化合物を含むことを特徴とする脂肪代謝改善剤、この脂肪代謝改善剤を含有するヒト 又は動物用医薬及び食品、並び該抽出液等を分離、精製することにより得ることができる新規メガスチグマン及びフラボノイド化合物。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、ベンケイソウ科(Crassulaceae)植物である垂盆草、その抽出物もしくは抽出エキス、又はこれらから得られるメガスチグマン化合物又 はフラボノイド化合物を含有する脂肪代謝改善剤、及びその脂肪代謝改善剤を含有する医薬や食品に関する。本発明は、さらに、垂盆草、その抽出物又は抽出エ キスから得られる新規メガスチグマン化合物及びフラボノイド化合物に関するものである。
【背景技術】
【0002】
垂盆草(学名:Sedum sarmentosum Bge.)は、多年生多肉質草本で、高さは10~20cm、茎は淡紅色で、枝は細く、斜めに伸び、ほふくし、花序に近いところにまた根が生じやすい。中国 の遼寧、河北、河南、山東、山西、陜西、四川、浙江、江蘇、安徽、江西、湖北、広西、雲南、貴州省などに分布し、その山間部の山肌の傾斜面もしくは岩石上 に自生している。垂盆草は和名をツルマンネングサと称し、またその全草は漢薬“石指甲(セキシコウ)”と称され、「清熱する、腫れを消す、解毒する、の効 能がある」等とされている(非特許文献1)。しかしながら従来は、垂盆草に関する詳細な含有成分の探索等の科学的研究はあまり実施されていなかった。この ような背景のもと、本発明者らは垂盆草含有成分の解明研究を行い、これまでに種々のメガスチグマン化合物、フラボノイド化合物及びその他の化合物を垂盆草 より単離した(非特許文献2~5)。
【非特許文献1】上海科学技術出版社編、中薬大辞典、小学館、1985、pp.1427-1428
【非特許文献2】Yoshikawa M.,et al.,J. Nat. Prod.,70,575-583(2007)
【非特許文献3】Morikawa T.,et al.,Chem. Pharm. Bull.,55,435-441(2007)
【非特許文献4】Zhang Y.,et al.,Heterocycles,71,1565-1576(2007)
【非特許文献5】Ninomiya K.,et al.,Chem. Pharm. Bull.,55,1185-1191(2007)
【発明の開示】
【発明が解決しようとする課題】
【0003】
本発明は、垂盆草に関する詳細な含有成分の探索、及びその薬剤としての作用についての研究に基づいてなされたもので、垂盆草より得られ、脂肪代謝改善作用 を有する薬剤(脂肪代謝改善剤)を提供することを目的とする。本発明は、又、この脂肪代謝改善剤を含有するヒト又は動物用医薬、及び、この脂肪代謝改善剤 を含有する食品を提供することを目的とする。本発明は、さらに、垂盆草より得ることができる新規メガスチグマン及びフラボノイド化合物を提供することを目 的とする。
【課題を解決するための手段】
【0004】
本発明者は、垂盆草の全草や、垂盆草を水や低級脂肪族アルコール等により抽出して得られた抽出液、又は当該抽出液を濃縮して得られる抽出エキスについて、 脂肪代謝改善剤としての活性評価の指標として、ヒト肝がん由来細胞であるHepG2細胞を用いた細胞内脂肪代謝促進作用を検討した。その結果、垂盆草の全 草、その抽出液、抽出エキスが、脂肪代謝改善作用を示すことを見出し、以下に示す態様の発明を完成した。
【0005】
即ち、本発明は、その第1の態様として、垂盆草の全草、水、低級脂肪族アルコールもしくは低級脂肪族アルコールの含水物により垂盆草を抽出して得られる抽 出液、又は前記抽出液を濃縮して得られる抽出エキス、を有効成分として含むことを特徴とする脂肪代謝改善剤(請求項1)を提供する。
【0006】
本発明者は、さらに、前記の抽出液又は抽出エキスを分離、精製し、含有成分の詳細な探索等を行うとともに、この分離、精製により得られた化合物について、 ヒト肝がん由来細胞であるHepG2細胞を用いた細胞内脂肪代謝促進作用を検討したところ、いくつかの化合物がこの脂肪代謝改善作用を示すことを見出し、 以下に示す態様の発明を完成した。
【0007】
即ち本発明は、その第2の態様として、
下記の構造式(1)で表わされるメガスチグマン化合物:
【0008】
【化1】
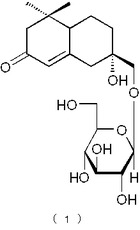
下記の構造式(3)で表わされるメガスチグマン化合物:
【0009】
【化2】
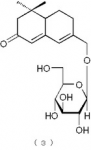
下記の構造式(4)で表わされるメガスチグマン化合物:
【0010】
【化3】
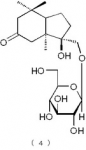
下記の構造式(7)で表わされるフラボノイド化合物:
【0011】
【化4】
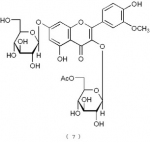
、及び下記の構造式(9)で表わされるフラボノイド化合物:
【0012】
【化5】
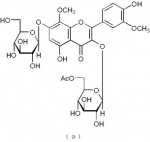
からなる群の中から選ばれる化合物を有効成分として含むことを特徴とする脂肪代謝改善剤(請求項2)を提供する。
【0013】
前記の第1の態様及び第2の態様の脂肪代謝改善剤は、脂肪代謝改善作用を有するため、これを含有させることにより、脂肪代謝改善作用を有する医薬や健康食 品等を得ることができる。即ち、本発明は、その第3の態様として、前記の第1の態様及び第2の態様の脂肪代謝改善剤を含有することを特徴とするヒト又は動 物用の医薬(請求項3)を提供する。又、その第4の態様として、前記の第1の態様及び第2の態様の脂肪代謝改善剤を含有することを特徴とする食品(請求項 4)を提供する。
【0014】
本発明者は、さらに又、前記の抽出液又は抽出エキスを分離、精製して得られた含有成分の中に、いくつかの新規なメガスチグマン化合物及びフラボノイド化合 物が含まれていることを見いだした。これらの新規化合物には、前記構造式(1)、(3)、(4)、(7)又は(9)で表わされる化合物が含まれ、又残余の 化合物もその構造の類似性から、脂肪代謝改善作用を有するものと推測される。
【0015】
即ち、本発明は、その第5の態様として、
構造式(1)で表わされるメガスチグマン化合物(請求項5)、
下記の構造式(2)で表わされるメガスチグマン化合物(請求項6):
【0016】
【化6】
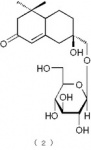
【0017】
構造式(3)で表わされるメガスチグマン化合物(請求項7)、
構造式(4)で表わされるメガスチグマン化合物(請求項8)、
下記の構造式(5)で表わされるメガスチグマン化合物(請求項9):
【0018】
【化7】
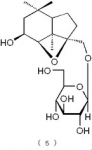
下記の構造式(6)で表わされるメガスチグマン化合物(請求項10):
【0019】
【化8】
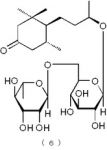
【0020】
構造式(7)で表わされるフラボノイド化合物(請求項11)、
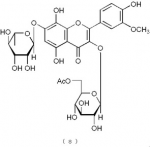
下記の構造式(8)で表わされるフラボノイド化合物(請求項12):
【0021】
【化9】
【0022】
及び、構造式(9)で表わされるフラボノイド化合物(請求項13)を提供する。
【発明の効果】
【0023】
本発明の第1の態様、即ち、垂盆草の全草、その水、低級脂肪族アルコールもしくはその含水物により抽出して得られる抽出液または当該抽出液を濃縮して得ら れる抽出エキスを有効成分として含有する脂肪代謝改善剤、又は、第2の態様、即ち、構造式(1)、(3)もしくは(4)で表されるメガスチグマン化合物、 又は構造式(7)もしくは(9)で表されるフラボノイド化合物を有効成分として含有する脂肪代謝改善剤は、ヒト肝がん由来細胞であるHepG2細胞を用い た細胞内脂肪代謝促進作用を示し、脂肪代謝改善剤としての優れた活性を有する。この脂肪代謝改善剤を含有させた医薬や食品(本発明の第3の態様、第4の態 様)は、優れた脂肪代謝改善効果を示す医薬又は食品である。さらに、本発明の第5の態様の新規なメガスチグマン化合物及びフラボノイド化合物は、前記のよ うな脂肪代謝改善作用を有するものであり、脂肪代謝改善剤として使用することができる。
【発明を実施するための最良の形態】
【0024】
次に、本発明を実施するための最良の形態につき説明するが、本発明の範囲はこの実施の形態のみに限定されるものではない。
【0025】
本発明の第1の態様の脂肪代謝改善剤としては、垂盆草の全草を用いたものを例示することができる。垂盆草の全草を用いる場合は、垂盆草の全草をそのまま用 いることができるし、又は、粉砕、破砕、切断、すりつぶしなどによる形状変化を行ったもの、もしくは、乾燥などの調製を実施したものを用いることもでき る。
【0026】
本発明の第1の態様の脂肪代謝改善剤としては、又、垂盆草を、水、低級脂肪族アルコールもしくは低級脂肪族アルコールの含水物により抽出して得られる抽出液、又はその抽出エキスを用いたものも例示することができる。
【0027】
この抽出液は、垂盆草の全草をそのまま、水、低級脂肪族アルコール及び低級脂肪族アルコールの含水物より選ばれる抽出溶媒により、抽出して得ることもでき るが、垂盆草の全草を、粉砕、破砕、切断、すりつぶしなどによる形状変化を行ったものを用いて抽出する方法が、抽出効率の面で好ましい。
【0028】
抽出溶媒として用いられるアルコールとしては、炭素数1~4の低級アルコール類が挙げられ、具体的には、メタノール、エタノール、プロパノール、イソプロ パノール、nブタノール、イソブタノール、t-ブタノール又はこれらの混液が挙げられる。抽出溶媒としては、好ましくはこれらのアルコール、又はこれらの アルコールに30容量%までの水を含有する含水アルコールが用いられる。前記のアルコールの中でもメタノール又はエタノールが好ましい。これらの抽出溶媒 は、抽出材料に対して、1~50倍(重量)程度、好ましくは10~30倍程度用いられる。
【0029】
抽出温度は、室温~溶媒の沸点の間で任意に設定できるが、例えば50℃~抽出溶媒の沸点の温度で、振盪下もしくは非振盪下または還流下に、前記の抽出材 料、即ち、垂盆草の全草、又は、それを粉砕、破砕、切断、すりつぶしなどによる形状変化を行ったもの等を、前記の抽出溶媒に浸漬することによって行うのが 適当である。
【0030】
好ましい抽出時間は、抽出温度や抽出の際の振盪の有無等により変動し、特に限定されない。例えば、抽出材料を振盪下に浸漬する場合には、30分間~10時 間程度行うのが適当であり、非振盪下に浸漬する場合には、1時間~20日間程度行うのが適当である。又、抽出溶媒の還流下に抽出するときは、30分間~数 時間加熱還流するのが好ましい。なお、50℃より低い温度で浸漬して抽出することも可能であるが、その場合には、前記の時間よりも長時間浸漬するのが好ま しい。抽出操作は、同一材料について1回だけ行ってもよいが、複数回、例えば2~5回程度繰り返すのが好ましい。
【0031】
前記の抽出工程により得られた抽出液には垂盆草の含有成分が溶出されている。本発明の脂肪代謝改善剤には、このようにして得られた抽出液をそのまま加えて もよいが、前記抽出液を濃縮して抽出エキスにして脂肪代謝改善剤としてもよい。濃縮は、低温で減圧下に行うのが好ましい。なお、濃縮する前に濾過して濾液 を濃縮してもよい。抽出エキスは、濃縮したままの状態で脂肪代謝改善剤として用いることができるが、また、濃縮は乾固するまで行ってもよく、粉末状又は凍 結乾燥品等として用いてもよい。濃縮する方法、粉末状及び凍結乾燥品とする方法は、当該分野での公知の方法を用いることができる。
【0032】
このようにして得られる抽出液又は抽出エキスを、精製処理に付し、含有される各成分に分離することができる。そして、分離された成分中には、脂肪代謝改善作用を有する化合物が含まれており、これらも脂肪代謝改善剤として用いることができる(本発明の第2の態様)。
【0033】
精製処理は、例えば、クロマトグラフ法、イオン交換樹脂を使用する溶離法、溶媒による分配抽出等を単独、又は組み合わせて採用することができる。クロマト グラフ法としては、順相クロマトグラフィー、逆相クロマトグラフィー、薄層クロマトグラフィー、遠心液体クロマトグラフィー、高速液体クロマトグラフィー 等を挙げることができ、これらのいずれか、又はそれらを組み合わせで行う方法が挙げられる。この際の担体、溶出溶媒等の精製条件は、各種クロマトグラ フィーに対応して適宣選択することができる。
【0034】
抽出液又は抽出エキスを、精製処理に付し、各成分に分離することにより、前記の構造式(1)~(9)のいずれかで表される新規化合物を得ることができ、それぞれ以下に示すように命名した。
【0035】
構造式(1)の化合物:セダモシドK(Sedumoside K)
構造式(2)の化合物:セダモシドL(Sedumoside L)
構造式(3)の化合物:セダモシドM(Sedumoside M)
構造式(4)の化合物:セダモシドN(Sedumoside N)
構造式(5)の化合物:セダモシドO(Sedumoside O)
構造式(6)の化合物:セダモシドJ(Sedumoside J)
構造式(7)の化合物:サルメノシドV(Sarmenoside V)
構造式(8)の化合物:サルメノシドVI(Sarmenoside VI)
構造式(9)の化合物:サルメノシドVII(Sarmenoside VII)
【0036】
前記のように、垂盆草の全草、水、低級脂肪族アルコールもしくは低級脂肪族アルコールの含水物により垂盆草を抽出して得られる抽出液、前記抽出液を濃縮し て得られる抽出エキス、及び、前記構造式(1)、(3)又は(4)で表わされる新規メガスチグマン化合物、構造式(7)又は(9)で表わされる新規フラボ ノイド化合物は、脂肪代謝改善剤としての活性評価の指標として実施したヒト肝がん由来細胞であるHepG2細胞を用いた細胞内脂肪代謝促進作用試験におい て、活性が見出された。
【0037】
この脂肪代謝改善試験は、ヒト肝がん由来細胞であるHepG2細胞を用い、高濃度グルコースを含む培地にて培養し細胞内に脂肪を蓄積させた後、低濃度グル コース含有培地へ交換するとともに被検サンプルを添加し、培養後の細胞内トリグリセリド残存量を脂肪代謝の指標として評価したものである。これにより、肝 細胞における脂肪代謝促進作用の高い検体は、肝臓における脂肪代謝を改善すると判断される。従って、垂盆草の全草、水、低級脂肪族アルコールもしくは低級 脂肪族アルコールの含水物により垂盆草を抽出して得られる抽出液、前記抽出液を濃縮して得られる抽出エキス、及び、前記構造式(1)、(3)又は(4)で 表わされる新規メガスチグマン化合物、構造式(7)又は(9)で表わされる新規フラボノイド化合物は、脂肪代謝改善剤として用いることができる。
【0038】
さらに、この本発明の脂肪代謝改善剤は、医薬や食品に適用することができ、この脂肪代謝改善剤を含有させることにより優れた脂肪代謝改善効果を有する医薬や食品を製造することができる。
【0039】
例えば、垂盆草の全草、水、低級脂肪族アルコールもしくは低級脂肪族アルコールの含水物により垂盆草を抽出して得られる抽出液、前記抽出液を濃縮して得ら れる抽出エキス、前記構造式(1)、(3)もしくは(4)で表わされる新規メガスチグマン化合物、又は構造式(7)もしくは(9)で表わされる新規フラボ ノイド化合物を、そのままの状態で又は適当な媒体で希釈して、医薬品等の製造分野における公知の方法により、散剤、顆粒剤、錠剤、カプセル剤又は液剤等の 種々の形態にして、医薬品として使用することができる。
【0040】
これらの形態においては、適当な媒体を添加してもよい。適当な媒体としては、医薬的に許容される賦形剤、例えば結合剤(例えばシロップ、アラビアゴム、ゼ ラチン、ソルビトール、トラガント又はポリビニルピロリドン)、充填剤(例えば乳糖、砂糖、トウモロコシ澱粉、リン酸カルシウム、ソルビトール又はグリシ ン)、錠剤用滑剤(例えばステアリン酸マグネシウム、タルク、ポリエチレングリコール又はシリカ)、崩壊剤(例えば馬鈴薯澱粉)又は湿潤剤(例えばラウリ ル硫酸ナトリウム)等が挙げられる。
【0041】
錠剤とする場合は、通常の製薬における周知の方法でコートしてもよい。液体製剤とする場合は、例えば水性又は油性の懸濁液、溶液、エマルジョン、シロップ又はエリキシルの形態であってもよい。又、使用前に水や他の適切な賦形剤と混合する乾燥製品として提供してもよい。
【0042】
こうした液体製剤は、通常の添加剤、例えば、ソルビトール、シロップ、メチルセルロース、グルコースシロップ、ゼラチン水添加食用脂等の懸濁化剤、レシチ ン、ソルビタンモノオレエート、アラビアゴム等の乳化剤(食用脂を含んでもよい)、アーモンド油、分画ココヤシ油又はグリセリン、プロピレングリコールや エチレングリコールのような油性エステル等の非水性賦形剤、p-ヒドロキシ安息香酸メチルもしくはプロピル又はソルビン酸等の保存剤、を含んでもよく、さ らに所望により着色剤又は香料等を含んでもよい。
【0043】
垂盆草の全草、水、低級脂肪族アルコールもしくは低級脂肪族アルコールの含水物により垂盆草を抽出して得られる抽出液、前記抽出液を濃縮して得られる抽出 エキス、前記構造式(1)、(3)もしくは(4)で表わされる新規メガスチグマン化合物、又は構造式(7)もしくは(9)で表わされる新規フラボノイド化 合物は、それぞれ単独で、又は混合物として食品に含有させ、食品に脂肪代謝改善効果を与えることができる。ここで言う食品には健康食品も含まれる。
【0044】
ここで健康食品とは、通常の食品よりも積極的な意味で、保健、健康維持・増進等を目的とした食品を意味する。食品又は健康食品の形態としては、例えば、液 体又は半固形、固形の製品、具体的には散剤、顆粒剤、錠剤、カプセル剤又は液剤等のほか、クッキー、せんべい、ゼリー、ようかん、ヨーグルト、まんじゅう 等の菓子類、清涼飲料、お茶類、栄養飲料、スープ等の形態が挙げられる。これらの食品の製造工程において、あるいは最終製品に、前記の抽出物、抽出エキ ス、及び/又は化合物を混合又は塗布、噴霧などにより添加して、健康食品とすることができる。
【0045】
本発明の医薬又は食品における、前記抽出液、抽出エキス、前記構造式(1)、(3)もしくは(4)で表わされる新規メガスチグマン化合物、又は構造式 (7)もしくは(9)で表わされる新規フラボノイド化合物の使用量は、濃縮、精製の程度、活性の強さ等、使用目的、対象疾患や自覚症状の程度、使用者の体 重、年齢等によって適宣調整される。例えば、医薬として成人について使用する場合は、1回の投与毎に、抽出液又は抽出エキスでは、1mg~20g程度の範 囲で使用し、この範囲内で精製度や水分含量等に応じて調整することが適当な場合が多い。又、前記化合物を使用する場合は、1mg~1g程度が適当な場合が 多い。
【0046】
又、健康食品として使用する場合は、食品の味や外観に悪影響を及ぼさない量、例えば、対象となる食品1kgに対して、前記の抽出液又は抽出エキス、前記構 造式(1)、(3)もしくは(4)で表わされる新規メガスチグマン化合物、又は構造式(7)もしくは(9)で表わされる新規フラボノイド化合物を、 1mg~20g程度の範囲で添加することが適当な場合が多い。
【0047】
なお、前記構造式(2)、(5)もしくは(6)で表わされる新規メガスチグマン化合物、又は構造式(8)で表わされる新規フラボノイド化合物も、その構造 の類似性から、前記構造式(1)、(3)もしくは(4)で表わされる新規メガスチグマン化合物、又は構造式(7)もしくは(9)で表わされる新規フラボノ イド化合物と同様に、脂肪代謝改善効果を有し、脂肪代謝改善剤として用いることができ、又、ヒトや動物の医薬品や、健康食品等の食品に添加して、脂肪代謝 改善効果を有する医薬品や食品を製造することができると考えられる。
【実施例】
【0048】
以下、実施例により、本発明をさらに具体的に説明するが、実施例は本発明の範囲を限定するものではない。なお、以下の実施例では、特に記載がない限り、以下の各種溶媒、濾紙、クロマトグラフィー用担体及びHPLCカラムを用いた。
【0049】
[溶媒]
メタノール:ナカライテスク社製、一級
クロロホルム:ナカライテスク社製、一級
HPLC用メタノール:関東化学社製、特級
HPLC用アセトニトリル:関東化学社製、特級
【0050】
[濾紙] アドバンテック社製:No.2
【0051】
[クロマトグラフィー用担体]
順相シリカゲルカラムクロマトグラフ用担体:富士シリシア社製、BW-200、150~300メッシュ
逆相ODSカラムクロマトグラフ用担体:富士シリシア社製、Chromatorex ODS1020T、100~200メッシュ
多孔質ポリマーカラムクロマトグラフ用担体:日本練水社製、ダイアイオンHP-20及びファルマシア社製、セファデックスLH-20
【0052】
[HPLCカラム]
YMC社製、YMC Pack-ODS-A、20mm(i.d.)×250mm
【0053】
実施例1 垂盆草全草の熱水抽出エキスの調製
新鮮な垂盆草の全草800kgを粉砕し、これに約10倍量の水(8000L)を加え、加熱還流下1時間抽出した。抽出後、ひだ折り濾紙で濾過した後、ロー タリーエバポレーターを用いて減圧下に、抽出液より溶媒を留去して、垂盆草(ツルマンネングサ)の熱水抽出エキス10kg(乾燥原料からの収率 1.25%)を得た。
【0054】
実施例2 熱水抽出エキスの分離及び精製
前記の熱水抽出エキス(1950g)に約10倍量のメタノール(20L)を加え、加熱還流下3時間抽出した。抽出後、ひだ折り濾紙で濾過した後、抽出残渣 に再度メタノール(50L)を加え、3時間加熱還流し、同様に濾過作業を行った。合計3回の抽出を行い、その抽出液をあわせ、ロータリーエバポレーターを 用いて、減圧下に溶媒を留去して、垂盆草のメタノール可溶性画分887.5g(原料からの収率0.57%)を得た。
【0055】
実施例3 メタノール可溶性画分の調製
前記メタノール可溶性画分(398.6g)を、多孔質ポリマーカラムカラムクロマトグラフィー(ダイアイオンHP-20:4.0kg,移動相:水→メタノール)で順次溶出し、水溶出部(305.0g)及びメタノール溶出部(93.6g)を得た。
【0056】
実施例4 メタノール溶出部の分離及び精製
前記メタノール溶出部(72.0g)を、順相シリカゲルカラムクロマトグラフィー(2.0kg、移動相:クロロホルム/メタノール/水 (10/3/0.5、下層→7/3/1,下層)→メタノール)で順次溶出し、溶出画分1(12.1g)、2(19.2g)、3(10.4g)、 4(8.7g)、5(16.3g)を得た。
【0057】
実施例5
このうち、溶出画分1(12.1g)について、逆相ODSカラムクロマトグラフィー(300g,移動相:メタノール/水 (5/95→10/90→20/80→30/70→50/50→70/30)→メタノール)、多孔質ポリマーカラムカラムクロマトグラフィー(セファデッ クスLH-20:150g,移動相:クロロホルム/メタノール(50/50))及びHPLC(移動相:メタノール/水(42/58))にて分離、精製し、 セダモシドM(sedumoside M,21.3mg,0.00004%)を得た。
【0058】
実施例6
溶出画分2(19.2g)について、逆相ODSカラムクロマトグラフィー(600g,移動相:メタノール/水 (20/80→30/70→40/60→70/30)→メタノール)、順相シリカゲルカラムクロマトグラフィー(100g,移動相:クロロホルム→クロロ ホルム/メタノール(50/1→20/1→10/1)→クロロホルム/メタノール/水(20/3/1,下層)→メタノール)もしくは多孔質ポリマーカラム カラムクロマトグラフィー(セファデックスLH-20:150g,移動相:クロロホルム/メタノール(50/50))、及びHPLC(移動相:メタノール /水(32/68又は40/60)又はアセトニトリル/メタノール/水(10/8/82又は20/8/72))にて分離、精製し、化合物セダモシド K(sedumoside K,25.4mg,0.00005%)、セダモシドL(sedumoside L,12.3mg,0.00002%)、セダモシドM(sedumoside M,32.9mg,0.00006%)、セダモシドN(sedumoside N,9.2mg,0.00002%)、セダモシドO(sedumoside O,8.1mg,0.00002%)及びセダモシドJ(sedumoside J,2.5mg,0.00001%)を得た。
【0059】
実施例7
溶出画分3(10.4g)について、逆相ODSカラムクロマトグラフィー(240g,移動相:メタノール/水 (10/90→20/80→30/70→40/60)→メタノール)、多孔質ポリマーカラムカラムクロマトグラフィー(セファデックス LH-20:150g,移動相:クロロホルム/メタノール(50/50))及びHPLC(移動相:メタノール/水(40/60))にて分離、精製し、サル メノシドV(sarmenoside V,16.4mg,0.00003%)、サルメノシドVI(sarmenoside VI,27.7mg,0.00005%)及びサルメノシドVII(sarmenoside VII,12.8mg,0.00002%)を得た。
【0060】
実施例8
溶出画分4(8.7g)について、逆相ODSカラムクロマトグラフィー(240g,移動相:メタノール/水 (10/90→20/80→30/70→40/60→50/50)→メタノール)、多孔質ポリマーカラムカラムクロマトグラフィー(セファデックス LH-20:150g,移動相:クロロホルム/メタノール(50/50))及びHPLC(移動相:メタノール/水(35/65))にて分離、精製し、サル メノシドVI(sarmenoside VI,21.2mg,0.00004%)を得た。
【0061】
前記の実施例で得られた構造式(1)~(9)で示される化合物についての、質量分析、赤外吸収スペクトル、核磁気共鳴スペクトル等の測定により得られた結果を以下に示す。なお、以下の1H-NMR及び13C-NMRによる構造解析に用いたナンバリングは、次式に基づいている。
【0062】
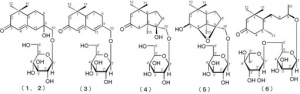
[構造式(1)~(6)の化合物について]
【0063】
【化10】
【0064】
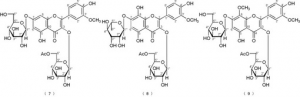
[構造式(7)~(9)の化合物について]
【0065】
【化11】
【0066】
セダモシドK(Sedumoside K:構造式(1)の化合物)の物性測定値
・性状: 不定形粉末
・旋光度:[α]D25: +40.0°(c=1.35,MeOH)
・紫外吸収スペクトル[MeOH,nm,(log ε)]:241(4.06)
・円二色性スペクトル(MeOH,nm,Δε):242(+2.92),283(0.02),319(+0.37)
・高分解能質量分析(High-resolution EI-MS):
理論値 C19H30O8 (M+) : 386.1940
実測値 : 386.1936
・赤外吸収スペクトル(KBr,cm1): 3389,1653,1076,1036
・質量分析EI-MS: m/z 386 (M+,3),368(6),206(86),190(92),178(13),148(100)
・核磁気共鳴スペクトル:
1H-NMR(500MHz,CD3OD):δ
0.95,1.06(3H each, both s,11,12-H3),1.43,1.95(1H each, both m,7β,7α-H),1.61(1H,ddd,J=4.0,13.1,13.4Hz,8α-H),2.15(1H,m,8β-H),2.19,2.25(1H each, both d, J=15.6Hz,2α,2β-H),2.23(1H,m,6-H),2.37(1H,d,J=13.9Hz,13α-H),2.70(1H,dd,J=2.1,13.9Hz,13β-H),3.22(1H,dd,J=7.7,9.2Hz,2′-H),3.25(1H,m,5′-H),3.26(1H,dd,J=8.6,8.6Hz,4′-H),3.36(1H,m,3′-H),3.39,3.78(1H each, both d, J=10.7Hz,10-H2),[3.65(1H,dd,J=5.5,11.4Hz),3.83(1H,dd,J=1.8,11.4Hz),6'-H2],4.25(1H,d,J=7.6Hz,1′-H),5.83(1H,br s,4-H)
13C-NMR(125MHz,CD3OD):δC
35.8(C-1),51.6(C-2),202.5(C-3),125.5(C-4),165.7(C-5),49.3(C-6),24.5(C-7),35.2(C-8),74.5(C-9),74.5(C-10),24.3(C-11),28.9(C-12),46.1(C-13),104.9(C-1′),75.2(C-2′),78.0(C-3′),71.6(C-4′),77.9(C-5′),62.7(C-6′)
【0067】
セダモシドL(Sedumoside L:構造式(2)の化合物)の物性測定値
・性状: 不定形粉末
・旋光度:[α]D25: +39.6°(c=1.90,MeOH)
・紫外吸収スペクトル[MeOH,nm,(log ε)]:241(4.10)
・円二色性スペクトル(MeOH,nm,Δε):239(+2.35),278(0.05),321(+0.42)
・高分解能質量分析(High-resolution EI-MS):
理論値 C19H30O8 (M+) : 386.1940
実測値 : 386.1934
・赤外吸収スペクトル(KBr,cm1): 3389,1653,1076,1037
・質量分析EI-MS: m/z 386 (M+,1),368(9),206(85),190(100),178(12),148(4)
・核磁気共鳴スペクトル:
1H-NMR(500MHz,CD3OD):δ
0.98,1.07(3H each, both s,11,12-H3),1.78,1.89(1H each, both m,7β,7α-H),1.74,1.81(1H each, both m,8α,8β-H),2.19,2.26(1H each, both d, J=15.6Hz,2α,2β-H),2.19(1H,m,6-H),2.48(1H,d,J=14.6Hz,13α-H),2.54(1H,dd,J=1.9,14.6Hz,13β-H),3.23(1H,dd,J=7.7,9.2Hz,2′-H),3.28(2H,m,4′,5′-H),3.36(1H,m,3′-H),3.40,3.83(1H each, both d, J=10.1Hz,10-H2),[3.65(1H,dd,J=5.5,11.9Hz),3.87(1H,dd,J=1.8,11.9Hz),6'-H2],4.29(1H,d,J=7.7Hz,1′-H),5.83(1H,br s,4-H)
13C-NMR(125MHz,CD3OD):δC
35.7(C-1),51.3(C-2),202.5(C-3),125.6(C-4),167.1(C-5),50.0(C-6),23.7(C-7),34.1(C-8),74.6(C-9),79.0(C-10),24.6(C-11),28.9(C-12),46.1(C-13),105.0(C-1′),75.2(C-2′),77.9(C-3′),71.6(C-4′),78.0(C-5′),62.7(C-6′)
【0068】
セダモシドM(Sedumoside M:構造式(3)の化合物)の物性測定値
・性状: 不定形粉末
・旋光度:[α]D27: 63.7°(c=1.00,MeOH)
・紫外吸収スペクトル[MeOH,nm,(log ε)]:290(4.12)
・円二色性スペクトル(MeOH,nm,Δε):283(2.63)
・高分解能質量分析(High-resolution positive-ion FAB-MS):
理論値 C19H28O7Na (M+Na)+ : 391.1733
実測値 : 391.1738
・赤外吸収スペクトル(KBr,cm1): 3649,1653,1576,1076
・質量分析
positive-ion FAB-MS: m/z 391 (M+Na)+
・核磁気共鳴スペクトル:
1H-NMR(500MHz,CD3OD):δ
0.88,1.15(3H each, both s,11,12-H3),1.45,2.05(1H each, both m,7β,7α-H),2.17(1H,dd,J=0.9,16.2Hz,2β-H),2.30,2.40(1H each. both m,8β,8α-H),2.44(1H,d,J=16.2Hz,2α-H),2.50(1H,m,6-H),3.23(1H,m,2′-H),3.26(1H,m,5′-H),3.28(1H,m,4′-H),3.36(1H,m,3′-H), [3.66(1H,dd,J=5.5,11.9Hz),3.86(1H,dd,J=2.1,11.9Hz),6'-H2],4.22,4.43(1H each, both d,J=14.7Hz,10-H2),4.29(1H,d,J=7.7Hz,1′-H),5.79(1H,br s,4-H),6.45(1H,s,13-H)
13C-NMR(125MHz,CD3OD):δC
37.3(C-1),54.7(C-2),202.8(C-3),123.8(C-4),159.7(C-5),46.9(C-6),23.4(C-7),28.2(C-8),151.8(C-9),72.7(C-10),20.3(C-11),29.0(C-12),126.5(C-13),104.0(C-1′),75.1(C-2′),78.1(C-3′),71.6(C-4′),78.0(C-5′),62.8(C-6′)
【0069】
セダモシドN(Sedumoside N:構造式(4)の化合物)の物性測定値
・性状: 不定形粉末
・旋光度:[α]D25: 27.6°(c=0.70,MeOH)
・円二色性スペクトル(MeOH,nm,Δε):282(0.76),317(+0.02)
・高分解能質量分析(High-resolution EI-MS):
理論値 C19H32O8 (M+) : 388.2097
実測値 : 388.2099
・赤外吸収スペクトル(KBr,cm1): 3389,1708,1076,1035
・質量分析EI-MS: m/z 388 (M+,4),226(45),208(96),195(60),151(100)
・核磁気共鳴スペクトル:
1H-NMR(500MHz,CD3OD):δ
0.97,1.05(3H each, both s,11,12-H3),1.10(3H,s,13-H3),1.64,1.71(1H each, both m,8α,8β-H),1.77(2H,m,7-H2),1.80(1H,m,6-H),1.88,2.43(1H each, both d, J=17.4Hz,2α,2β-H),2.09,2.83(1H each, both d, J=17.7Hz,4α,4β-H),3.23(1H,dd,J=7.7,9.2Hz,2′-H),3.27(2H,m,4′,5′-H),3.35(1H,dd,J=9.2,9.2Hz,3′-H),3.48,4.04(1H each, both d, J=10.5Hz,10-H2),[3.65(1H,dd,J=5.8,11.9Hz),3.86(1H,dd,J=1.5,11.9Hz),6'-H2],4.22(1H,d,J=7.7Hz,1′-H)
13C-NMR(125MHz,CD3OD):δC
34.7(C-1),48.8(C-2),217.3(C-3),46.8(C-4),48.8(C-5),56.9(C-6),26.7(C-7),34.7(C-8),84.8(C-9),75.3(C-10),28.3(C-11),30.4(C-12),29.5(C-13),105.0(C-1′),75.1(C-2′),78.0(C-3′),71.7(C-4′),78.1(C-5′),62.8(C-6′)
【0070】
セダモシドO(Sedumoside O:構造式(5)の化合物)の物性測定値
・性状: 不定形粉末
・旋光度:[α]D25: 36.9°(c=0.41,MeOH)
・高分解能質量分析(High-resolution EI-MS):
理論値 C19H32O8 (M+) : 388.2097
実測値 : 388.2102
・赤外吸収スペクトル(KBr,cm1): 3389,1385,1075,1045
・質量分析EI-MS: m/z 388 (M+,1),370(2),226(21),209(100),191(77)
・核磁気共鳴スペクトル:
1H-NMR(500MHz,CD3OD):δ
0.96,0.97(3H each, both s,11,12-H3),1.21(3H,s,13-H3),1.29(1H,dd,J=5.8,12.8Hz,2α-H),1.59(ddd, J=8.0,12.5,14.1Hz,8α-H),1.66(1H,dd,J=8.6,10.4Hz,6-H),1.74(1H,dd,J=7.7,14.1Hz,8β-H),1.81,2.01(1H each, both m,7α,7β-H),1.87(1H,dd,J=12.8,12.8Hz,2β-H),3.22(1H,dd,J=7.7,9.2Hz,2′-H),3.28(2H,m,4′,5′-H),3.37(1H,dd,J=9.2,9.2Hz,3′-H),3.76,4.19(1H each, both d, J=11.0Hz,10-H2),3.77(1H,ddd,J=0.4,5.8,12.8Hz,3-H),[3.66(1H,ddd,J=1.2,4.3,11.9Hz),3.87(1H,dd,J=1.8,11.9Hz),6'-H2],4.33(1H,d,J=7.7Hz,1′-H),4.69(1H,d,J=4.0Hz,4-H)
13C-NMR(125MHz,CD3OD):δC
35.4(C-1),36.5(C-2),67.7(C-3),83.5(C-4),50.1(C-5),55.4(C-6),28.3(C-7),34.4(C-8),97.4(C-9),71.3(C-10),28.6(C-11),30.5(C-12),20.7(C-13),104.8(C-1′),75.3(C-2′),78.1(C-3′),71.8(C-4′),78.1(C-5′),62.9(C-6′)
【0071】
セダモシドJ(Sedumoside J:構造式(6)の化合物)の物性測定値
・性状: 不定形粉末
・旋光度:[α]D21: +22.9°(c=0.06,MeOH)
・円二色性スペクトル(MeOH,nm,Δε):290(+0.05)
・高分解能質量分析(High-resolution positive-ion FAB-MS):
理論値 C25H44O11Na (M+Na)+ : 543.2781
実測値 : 543.2786
・赤外吸収スペクトル(KBr,cm1): 3389,1706,1067,1047
・質量分析
positive-ion FAB-MS: m/z 543 (M+Na)+
・核磁気共鳴スペクトル:
1H-NMR(500MHz,CD3OD):δ
0.77,1.07(3H each, both s,11,12-H3),1.09(3H,d,J=6.1Hz,13-H3),1.14(1H,m,6-H),1.20(3H,d,J=6.1Hz,10-H3),1.20,1.64(1H each, both m,7-H2),1.26(3H,d,J=6.1Hz,6”-H3),1.65,1.72(1H each, both m,8-H2),1.96(1H,dd,J=2.5,13.2Hz,2β-H),2,19(1H,dd,J=12.2,12.2Hz,4α-H),2.22(1H,ddd,J=2.5,4.9,12.2Hz,4β-H),2,39(1H,d,J=13.2Hz,2α-H),3.14(1H,dd,J=7.3,8.6Hz,2′-H),3.23(1H,dd,J=8.5,8.5Hz,4′-H),3.32(1H,m,3′-H),3.36(1H,m,4”-H),3.38(1H,m,5′-H), [3.57(1H,dd,J=6.1,11.0Hz),3.97(1H,dd,J=2.5,11.0Hz),6''-H2],3.64(1H,m,5”-H),3.66(1H,m,3”-H),3.79(1H,m,9-H),3.81(1H,m,2”-H),4.30(1H,d,J=7.3Hz,1′-H), 4.74(1H,br s,1”-H)
13C-NMR(125MHz,CD3OD):δC
40.5(C-1),57.2(C-2),214.6(C-3),50.9(C-4),37.7(C-5),53.7(C-6),26.0(C-7),40.4(C-8),76.5(C-9),20.1(C-10),21.3(C-11),30.4(C-12),21.6(C-13),102.5(C-1′),75.2(C-2′),78.2(C-3′),72.0(C-4′),76.9(C-5′),68.6(C-6′),102.4(C-1”),72.3(C-2”),72.5(C-3”),74.0(C-4”),69.8(C-5”),18.2(C-6”)
【0072】
サルメノシドV(Sarmenoside V:構造式(7)の化合物)の物性測定値
・性状: 不定形黄色粉末
・旋光度:[α]D26: +30.2°(c=0.78,MeOH)
・紫外吸収スペクトル[MeOH,nm,(log ε)]:255(4.29),355(4.13)
・高分解能質量分析(High-resolution positive-ion FAB-MS):
理論値 C30H34O18Na (M+Na)+ : 705.1643
実測値 : 705.1640
・赤外吸収スペクトル(KBr,cm1): 3389,1718,1653,1603,1558,1456,1075
・質量分析
positive-ion FAB-MS: m/z 705 (M+Na)+
・核磁気共鳴スペクトル:
1H-NMR(500MHz,DMSO-d6):δ
1.74(3H,s,6”-OAc),3.87(3H,s,3′-OCH3),5.08(1H,d, J=7.5Hz,1”’-H),5.45(1H,d,J=7.6Hz,1”-H),6.48,6.84(1H each, both br s,6,8-H),6.93(1H,d,J=8.4Hz,5′-H),7.59(1H,dd,J=2.4,8.4Hz,6′-H),7.86(1H,d,J=2.4Hz,2′-H),12.57(1H,br s,5-OH)
13C-NMR(125MHz,DMSO-d6):δC
156.8(C-2),133.2(C-3),177.4(C-4),160.1(C-5),99.3(C-6),162.8(C-7),94.6(C-8),155.9(C-9),105.5(C-10),120.7(C-1′),113.2(C-2′),146.8(C-3′),149.6(C-4′),115.1(C-5′),122.4(C-6′),100.9(C-1”),74.1(C-2”),76.3(C-3”),69.7(C-4”),73.8(C-5”),62.5(C-6”),99.8(C-1”’),73.0(C-2”’),76.0(C-3”’),69.5(C-4”’),77.1(C-5”’),60.5(C-6”’),55.6(OCH3),20.0,169.8(OAc)
【0073】
サルメノシドVI(Sarmenoside VI:構造式(8)の化合物)の物性測定値
・性状: 不定形黄色粉末
・旋光度:[α]D27: +140.3°(c=1.15,MeOH)
・紫外吸収スペクトル[MeOH,nm,(log ε)]:258(4.08),274(4.08),344(3.94)
・高分解能質量分析(High-resolution positive-ion FAB-MS):
理論値 C28H32O17Na (M+Na)+ : 663.1537
実測値 : 663.1542
・赤外吸収スペクトル(KBr,cm1): 3389,1653,1609,1541,1458,1059
・質量分析
positive-ion FAB-MS: m/z 663 (M+Na)+
・核磁気共鳴スペクトル:
1H-NMR(500MHz,DMSO-d6):δ
1.13(3H,d,J=6.2Hz,6”’-H3),3.85(3H,s,3′-OCH3),5.51(1H,d,J=1.4Hz,1”’-H),5.57(1H,d,J=7.6Hz,1”-H),6.62(1H,br s,6-H),6.94(1H,d,J=8.3Hz,5′-H),7.64(1H,dd,J=2.1,8.3Hz,6′-H),7.99(1H,d,J=2.1Hz,2′-H),12.03(1H,br s,5-OH)
13C-NMR(125MHz,DMSO-d6):δC
156.6(C-2),132.9(C-3),177.8(C-4),152.0(C-5),98.7(C-6),150.4(C-7),126.9(C-8),144.4(C-9),105.4(C-10),121.1(C-1′),113.4(C-2′),146.8(C-3′),149.4(C-4′),115.1(C-5′),122.4(C-6′),100.6(C-1”),74.2(C-2”’),76.3(C-3”),69.8(C-4”),77.3(C-5”),60.5(C-6”),99.1(C-1”’),69.7(C-2”’),69.9(C-3”’),71.6(C-4”’),69.7(C-5”’),17.8(C-6”’),55.5(OCH3)
【0074】
サルメノシドVII(Sarmenoside VII:構造式(9)の化合物)の物性測定値
・性状: 不定形黄色粉末
・旋光度:[α]D27: -9.0°(c=0.54,MeOH)
・紫外吸収スペクトル[MeOH,nm,(log ε)]:257(4.22),358(4.05)
・高分解能質量分析(High-resolution positive-ion FAB-MS):
理論値 C31H36O19Na (M+Na)+ : 735.1748
実測値 : 735.1752
・赤外吸収スペクトル(KBr,cm1): 3420,1720,1653,1601,1559,1456,1071
・質量分析
positive-ion FAB-MS: m/z 735 (M+Na)+
・核磁気共鳴スペクトル:
1H-NMR(500MHz,DMSO-d6):δ
1.74(3H,s,OAc),3.87.3.87(3H each, both s,8,3′-OCH3),5.08(1H,d,J=7.6Hz,1”’-H),5.45(1H,d,J=7.6Hz,1”-H),6.68(1H,br s,6-H),6.96(1H,d,J=8.3Hz,5′-H),7.60(1H,dd,J=2.0,8.3Hz,6′-H),7.90(1H,d,J=2.0Hz,2′-H),12.28(1H,br s,5-OH)
13C-NMR(125MHz,DMSO-d6):δC
156.5(C-2),133.1(C-3),177.6(C-4),155.6(C-5),98.5(C-6),156.0(C-7),128.9(C-8),147.9(C-9),105.1(C-10),120.8(C-1′),113.1(C-2′),146.8(C-3′),149.8(C-4′),115.3(C-5′),122.2(C-6′),101.1(C-1”),74.1(C-2”),76.5(C-3”),69.7(C-4”),73.8(C-5”),62.6(C-6”),100.2(C-1”’),73.0(C-2”’),76.0(C-3”’),69.5(C-4”’),77.1(C-5”’),60.5(C-6”’),55.4,61.2(OCH3),20.0,169.7(OAc)
【0075】
実施例9 HepG2細胞を用いた脂肪代謝促進作用試験
実施例3で得られたメタノール溶出部、水溶出部、実施例5で得られたセダモシドM(構造式(3)の化合物)、実施例6で得られたセダモシドK(構造式 (1)の化合物)、セダモシドN(構造式(4)の化合物)、実施例7で得られたサルメノシドV(構造式(7)の化合物)、サルメノシドVII(構造式 (9)の化合物)について、脂肪代謝改善作用の指標として、HepG2細胞を用いた細胞内脂肪代謝促進作用試験を実施した。試験方法を以下に示す。
【0076】
大日本住友製薬社より購入したヒト肝がん由来HepG2細胞を用いた。培地はminimum essential medium Eagle(MEM,シグマ-アルドリッチ社)に10%(v/v)fatal calf serum(FCS)及び100units/mLペニシリンG、100μg/mLストレプトマイシン及び0.1mM非必須アミノ酸(インビトロジェン社) を添加して使用した。細胞の培養は、75cm2培養フラスコ(ファルコン社)中で行い、5%CO2雰囲気下37℃にて行った。継代操作は,培養した細胞をダルベッコPBS(-)(日水製薬社)で洗浄した後、0.02%(w/v)トリプシン(ディフコ社)及び0.05%(w/v)EDTA・2Na(同人化学社)を含むPBS(-)により剥離して、定法に従い行った。
【0077】
HepG2細胞を105cells/well(200μL/well) の細胞密度で48穴培養プレート(住友ベークライト社)に播種して実験を行った。培養1日後、被験サンプルを含む高濃度グルコース(4500mg/L)含 有DMEM(200μL/well)に培地交換して計6日間(2日に1回培地を交換)培養した。高濃度グルコース含有DMEMによる培養終了後、被験サン プルを添加した低濃度グルコース(1000mg/L)含有DMEM(200μL/well)に培地交換して、さらに20時間培養した。
【0078】
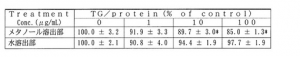
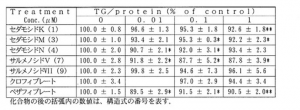
培養期間終了後、培養上清を除去、次いで蒸留水(100μL/well)を加え、超音波破砕機にて細胞を破砕した後、培養プレートを遠心分離 (3000rpm,10min,r.t.)に付し細胞破砕液を得た。得られた細胞破砕液の中性脂肪濃度及びタンパク質濃度は、それぞれ市販キットであるトリグリセリドEテストワコー(和光純薬工業社)及びBCAprotein assay kit(Pierce社)を使用して定量した。尚、定量結果については、タンパク質あたりの中性脂肪量(下表のTG/Protein)で算出し、対照群に 対する相対値(% of control)として表した。
【0079】
【表1】
【0080】
【表2】
【0081】
前記表1及び表2中の値は、平均値±標準誤差(N=4)で表記し、末尾の符号「*」および「**」は、Dunnettの多重比較検定で検定した対照との有意差:pが0.05および0.01未満であったことを表す。
【0082】
表1及び表2の結果より、垂盆草の全草の熱水抽出エキスのメタノール可溶性画分を、多孔質ポリマーカラム(ダイアイオンHP-20)を通じて調製したメタ ノール溶出部及び水溶出部、及び構造式(1)、(3)、(4)、(7)及び(9)で表される化合物は、HepG2細胞を用いた脂肪代謝促進作用試験におい て有意な脂肪代謝改善作用あるいは脂肪代謝改善傾向を有することがわかる。また、脂肪代謝促進作用試験において有意な脂肪代謝改善作用あるいは脂肪代謝改 善傾向を有した化合物に構造類似の、構造式(2)、(5)及び(6)で表されるメガスチグマン化合物、構造式(8)で表されるフラボノイド化合物について も、同様の作用を有すると推定される。
【0083】
とりわけ、構造式(1)のセダモシドK及び構造式(3)のセダモシドLは、市販抗高脂血症薬であるPPAR-γアゴニストのクロフィブレートよりも強力な脂肪代謝改善効果を有することが判明した。
【特許請求の範囲】
【請求項1】
垂盆草の全草、水、低級脂肪族アルコールもしくは低級脂肪族アルコールの含水物により垂盆草を抽出して得られる抽出液、又は前記抽出液を濃縮して得られる抽出エキス、を有効成分として含むことを特徴とする脂肪代謝改善剤。
【請求項2】
下記の構造式(1)で表わされるメガスチグマン化合物:
【化1】
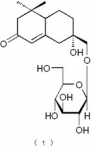
下記の構造式(3)で表わされるメガスチグマン化合物:
【化2】
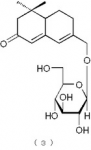
下記の構造式(4)で表わされるメガスチグマン化合物:
【化3】
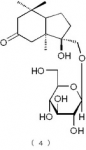
下記の構造式(7)で表わされるフラボノイド化合物:
【化4】
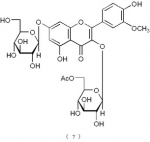
、及び下記の構造式(9)で表わされるフラボノイド化合物:
【化5】
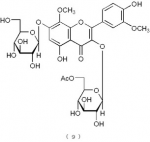
からなる群の中から選ばれる化合物を有効成分として含むことを特徴とする脂肪代謝改善剤。
【請求項3】
請求項1又は請求項2に記載の脂肪代謝改善剤を含有することを特徴とするヒト又は動物用の医薬。
【請求項4】
請求項1又は請求項2に記載の脂肪代謝改善剤を含有することを特徴とする食品。
【請求項5】
下記の構造式(1):
【化6】
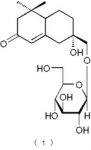
で表されるメガスチグマン化合物。
【請求項6】
下記の構造式(2):
【化7】
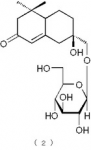
で表されるメガスチグマン化合物。
【請求項7】
下記の構造式(3):
【化8】
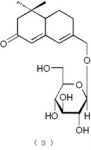
で表されるメガスチグマン化合物。
【請求項8】
下記の構造式(4):
【化9】
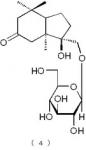
で表されるメガスチグマン化合物。
【請求項9】
下記の構造式(5):
【化10】
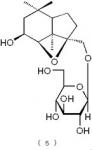
で表されるメガスチグマン化合物。
【請求項10】
下記の構造式(6):
【化11】
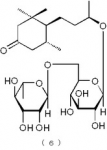
で表されるメガスチグマン化合物。
【請求項11】
下記の構造式(7):
【化12】
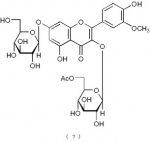
で表されるフラボノイド化合物。
【請求項12】
下記の構造式(8):
【化13】
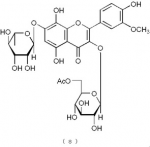
で表されるフラボノイド化合物。
【請求項13】
下記の構造式(9):
【化14】
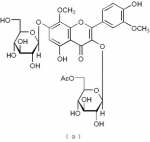
で表されるフラボノイド化合物。
【公開番号】特開2009-209045(P2009-209045A)
【公開日】平成21年9月17日(2009.9.17)
【国際特許分類】
生活必需品 | 医学または獣医学;衛生学 | 医薬用,歯科用又は化粧用製剤 | 藻類,地衣類,菌類もしくは植物又はそれらの派生物からの物質を含有する構造未知の医薬品製剤 | 被子植物門
生活必需品 | 医学または獣医学;衛生学 | 医薬用,歯科用又は化粧用製剤 | 藻類,地衣類,菌類もしくは植物又はそれらの派生物からの物質を含有する構造未知の医薬品製剤
生活必需品 | 医学または獣医学;衛生学 | 化合物または医薬製剤の特殊な治療活性 | 代謝系疾患の治療薬 | 高脂血症治療剤
生活必需品 | 医学または獣医学;衛生学 | 医薬用,歯科用又は化粧用製剤 | 有機活性成分を含有する医薬品製剤 | 炭水化物;糖;その誘導体 | グリコシド結合により,糖類でない化合物と結合した糖類基を持つ化合物
生 活必需品 | 医学または獣医学;衛生学 | 医薬用,歯科用又は化粧用製剤 | 有機活性成分を含有する医薬品製剤 | 炭水化物;糖;その誘導 体 | 糖類基と複素環とを持つ化合物 | 環構成異種原子として酸素原子を持つもの,例.ロイコグルコサン,へスペリジン,エリスロマイシン,ナイスタ チン
化学;冶金 | 有機化学 | 糖類;その誘導体;ヌクレオシド;ヌクレオチド;核酸 | 糖類基の異種原子に直接結合する炭化水素または置換炭化水素基を含有する化合物 | 炭素環で置換された非環式基
化学;冶金 | 有機化学 | 糖類;その誘導体;ヌクレオシド;ヌクレオチド;核酸 | 糖類基の異種原子に直接結合する炭化水素または置換炭化水素基を含有する化合物 | 複素環で置換された非環式または炭素環式基
化 学;冶金 | 有機化学 | 糖類;その誘導体;ヌクレオシド;ヌクレオチド;核酸 | 糖類基の異種原子に直接結合する複素環式基を含有する化合 物 | 異項原子として酸素のみを含有する複素環式化合物 | ベンゾピラン基 | ベンゾ〔b〕ピラン | ベンゾ〔b〕ピラン-4-オン
生 活必需品 | 食品または食料品;他のクラスに包含されないそれらの処理 | A21DまたはA23BからA23Jまでに包含されない食品,食料品,また は非アルコール性飲料;その調製または処理,例.加熱調理,栄養改善,物理的処理 | 食品または食料品;その調整または処理 | 食品の栄養改善;ダイ エット用製品 | 添加物を含有するもの
【出願番号】特願2008-50450(P2008-50450)
【出願日】平成20年2月29日(2008.2.29)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 発行者 :日本生薬学会 刊行物名:日本生薬学会第54回年会 名古屋(2007)講演要旨集 発行日 :2007年9月1日
【出願人】(000125347)学校法人近畿大学
【出願人】(503462394)株式会社栄進商事
【Fターム(参考)】
食品の着色及び栄養改善 | 栄養改善物質・菌類 | 有機化合物 | 水酸基を有するもの
食品の着色及び栄養改善 | 栄養改善物質・菌類 | 植物、植物由来のもの | 野草、薬草、スパイス
食品の着色及び栄養改善 | 目的・用途 | 血中脂質改善・血圧降下
食品の着色及び栄養改善 | 製造・処理 | 分離・抽出
糖類化合物 | C、H、Oのみからなる糖 | 単糖類
糖類化合物 | C、H、Oのみからなる糖 | 二糖類
糖類化合物 | 非糖類基の結合位置 | セミアセタール水酸基(1位)
糖類化合物 | 異種原子に直結する(非)置換炭化水素 | 炭素環で置換された非環式基
糖類化合物 | 異種原子に直結する(非)置換炭化水素 | 複素環で置換された非環式又は炭素環式基
糖類化合物 | 異種原子に直結する複素環 | Oのみ含有 | ベンゾピラン環 | ベンゾ〔b〕ピラン | ベンゾ〔b〕ピラン-4-オン
他の有機化合物及び無機化合物含有医薬 | 発明の種類 | 医薬の用途
他の有機化合物及び無機化合物含有医薬 | 発明の種類 | 医薬用途、薬理作用機序等の試験データあり
他の有機化合物及び無機化合物含有医薬 | 発明の種類 | 化学物質
他の有機化合物及び無機化合物含有医薬 | 炭水化物、糖類 | 単糖類、二糖、オリゴ糖(糖類基~6個) | 糖類基の異種原子に炭化水素基、複素環式基直結 | 糖類の異種原子に環式置換の非環式基直結
他の有機化合物及び無機化合物含有医薬 | 炭水化物、糖類 | 単糖類、二糖、オリゴ糖(糖類基~6個) | 糖類基の異種原子に炭化水素基、複素環式基直結 | 糖類の異種原子に複素環が直接結合
他の有機化合物及び無機化合物含有医薬 | 配合剤、剤型、適用部位 | 配合成分が1成分のもの
他の有機化合物及び無機化合物含有医薬 | 配合剤、剤型、適用部位 | 配合成分が2成分のもの
他の有機化合物及び無機化合物含有医薬 | 配合剤、剤型、適用部位 | 配合成分が3以上のもの
他の有機化合物及び無機化合物含有医薬 | 配合剤、剤型、適用部位 | クレームに薬効成分のみを記載
他の有機化合物及び無機化合物含有医薬 | 配合剤、剤型、適用部位 | 適用部位 | 経口
他の有機化合物及び無機化合物含有医薬 | 化合物自体又は配合、製剤化の目的、効果 | 新薬効の発現
他の有機化合物及び無機化合物含有医薬 | 医薬用途・機能・機作・対象・その他 | 生体機能への作用で特定された医薬 | 代謝系用薬 | 脂質代謝系用剤
植物物質含有医薬 | 活性成分の起源、由来となる種子植物 | 被子植物 | 双子葉植物
植物物質含有医薬 | 植物の薬用部分 | 全草又は樹木
植物物質含有医薬 | 単離された活性成分(物質) | 有機系活性成分 | 植物材料の | 抽出物(エキス)
植物物質含有医薬 | 単離された活性成分(物質) | 有機系活性成分 | 植物材料の | 抽出物(エキス) | 水抽出物
植物物質含有医薬 | 単離された活性成分(物質) | 有機系活性成分 | 植物材料の | 抽出物(エキス) | アルコール抽出物
植物物質含有医薬 | 単離された活性成分(物質) | 有機系活性成分 | 活性物質 | 糖類 | 配糖体の
植物物質含有医薬 | 単離された活性成分(物質) | 有機系活性成分 | 活性物質 | 糖類 | 配糖体の | フラボン系の
植物物質含有医薬 | 活性成分の分離、精製又は安定化の手段 | 機械的又は物理的処理 | 抽出によるもの
植物物質含有医薬 | 活性成分の分離、精製又は安定化の手段 | 機械的又は物理的処理 | 抽出によるもの | 親水性溶媒による抽出
植物物質含有医薬 | 活性成分の分離、精製又は安定化の手段 | 機械的又は物理的処理 | 抽出によるもの | 親水性溶媒による抽出 | 水のみによるもの
植物物質含有医薬 | 活性成分の分離、精製又は安定化の手段 | 機械的又は物理的処理 | 抽出によるもの | 親水性溶媒による抽出 | 低級アルコール類によるもの
植物物質含有医薬 | 活性成分の分離、精製又は安定化の手段 | 機械的又は物理的処理 | 濃縮又は乾燥又は凍結によるもの
植物物質含有医薬 | 配合剤、剤型、適用部位 | 適用部位 | 経口
植物物質含有医薬 | 物質自体又は配合、製剤化の目的・効果 | 新薬効の発現
植物物質含有医薬 | 医薬用途・機能・機作・対象・その他 | 生体機能への作用で特定された医薬 | 代謝系用薬 | 脂質代謝系用剤

![[商品価格に関しましては、リンクが作成された時点と現時点で情報が変更されている場合がございます。] [商品価格に関しましては、リンクが作成された時点と現時点で情報が変更されている場合がございます。]](https://hbb.afl.rakuten.co.jp/hgb/0ee64bac.09eec55d.0ee64bad.1e44806d/?me_id=1265514&item_id=10000008&pc=https%3A%2F%2Fthumbnail.image.rakuten.co.jp%2F%400_mall%2Fogimachilabo%2Fcabinet%2Fitems%2Fsuibonsou%2F11001-s1.jpg%3F_ex%3D240x240&s=240x240&t=picttext)

![[商品価格に関しましては、リンクが作成された時点と現時点で情報が変更されている場合がございます。] [商品価格に関しましては、リンクが作成された時点と現時点で情報が変更されている場合がございます。]](https://hbb.afl.rakuten.co.jp/hgb/0ee64bac.09eec55d.0ee64bad.1e44806d/?me_id=1265514&item_id=10000008&pc=https%3A%2F%2Fthumbnail.image.rakuten.co.jp%2F%400_mall%2Fogimachilabo%2Fcabinet%2Fitems%2Fsuibonsou%2F11001-s1.jpg%3F_ex%3D128x128&s=128x128&t=picttext)
Leave a Comment